![]() Bengt
Nordénnek, a Kémiai Nobel Bizottság tagjának szakmai véleménye a díjazott
munkájáról
Bengt
Nordénnek, a Kémiai Nobel Bizottság tagjának szakmai véleménye a díjazott
munkájáról
Idődtől és érdeklődésedtől függően a következő témák közül választhatsz:
Az 1999. évi kémiai Nobel-díj odaítélése
Bengt Nordénnek, a Kémiai Nobel Bizottság tagjának szakmai véleménye a díjazott munkájáról
Ahmed H. Zewail, California
Institute of Technology, Pasadena, USA
professzornak ítélte

az ún. femtokémia (más néven ultragyors jelenségek kémiája) megalapozásában
elért eredményeiért, átmeneti komplexek tanulmányozásáért ultragyors lézerek
segítségével. A femtokémia segítségével a kémiai reakciók egyes lépéseiről
kaphatunk képet, hiszen lehetővé vált femtoszekundum (1fs = 10-15s)
nagyságrendű folyamatok vizsgálata is.
Ahmed Zewail 1946-ban született Egyiptomban. Egyetemi tanulmányait szülőhazájában végezte az Alexandriai Egyetemen. Ezt követően az Egyesült Államokban, a Pennsylvaniai Egyetemen szerzett PhD fokozatot 1974-ben. Két évvel később Linus Pauling "székében" folytatta pályafutását a University of California (Berkeley) egyetem tanáraként 1990-ig. Zewail egyiptomi, amerikai kettős állampolgár.
Az oldal forrása: http://www.sulinet.hu/cgi-bin/db2www/lm/frame/cikk?id=1000&kat=bnb
A vegyészek már régóta törekszenek a kémiai reakciók legapróbb részleteinek tanulmányozására. Az idei kémiai Nobel-díjjal kitüntetett munka módot ad arra, hogy az atomok és molekulák mozgását "lassított felvétellel" kövessük nyomon a kémiai reakciók során.
Ahmed Zewail eljárását a világ leggyorsabb fényképészeti módszerének nevezhetjük. A vizsgálatok olyan rövid lézerimpulzusokra épülnek, amelyek a reakciók lejátszódásának időtartományába, a femtoszekundumos tartományba esnek. Egy femtoszekundum 1015 másodperc akkora a másodperchez képest, mint a másodperc a 32 millió évhez képest! A fizikai kémiának azt a területét, amely a femtoszekundumos folyamatokat vizsgálja, femtokémiának nevezik.
Száz év kutatás
Mindannyian tudjuk, hogy a kémiai reakciók nagyon eltérő sebességgel
zajlanak le gondoljunk csak a rozsdásodó szögre és robbanó dinamitra.
A reakciók többségében közös, hogy a hőmérséklet emelése élénkebb mozgásra
készteti a molekulákat, s ezzel megnöveli a folyamatok sebességét. Ezért
már régóta feltételezték, hogy a molekulákat "aktiválni kell"
"át kell lökni" egy gát fölött. Ezt a gátat a molekulák atomjait
összetartó erők szabják meg. Eddig azonban nagyon keveset tudtunk arról,
hogy a molekula hogyan küzdi le a gátat és milyen a gát tetején, az "átmeneti
állapotban".
A svéd fiziko-kémikus, Svante Arrhenius 1889-ben írta le először, hogy a kémiai reakciók sebessége hogyan változik a hőmérséklet függvényében. A kémiai sebességi állandóra (k) levezetett képletét
k = A eEa/kT
több mint egy évszázada használják a vegyészek (az exponensben k a Boltzmann-állandó, T a hőmérséklet kelvinben, Ea az aktiválási energia: a gát magassága addig a feltételezett állapotig, amelyet Arrhenius "aktivált komplex"-nek nevezett).
Az összefüggés értelmezését az 1930-as években terjeszették ki, amikor Henry Eyring és Michael Polanyi egymástól függetlenül dolgozta ki a mikroszokopikus rendszerek (molekulák) dinamikáján alapuló "átmeneti állapot elmélet"-et, és összefüggést adott meg az exponenciális előtt álló A tényezőre. Az elmélet egyik feltevése az volt, hogy az átmeneti állapoton nagyon gyorsan, a molekularezgések idejéhez hasonló idő alatt jutnak át a részecskék. Arról azonban senki sem álmodott, hogy ilyen rövid időtartamú kísérleteket is végeznek majd.
Pedig Ahmed Zewail éppen ezt teszi, mióta az alacsony hőmérsékletű antracénmolekulák
vizsgálata során, az 1970-es években, rájött, hogy a molekulákat arra késztethetjük,
hogy egyszerre rezegjenek. Kísérleteiben kulcsfontosságú szerepet játszanak
a "koherens preparátumok" A femtokémia kialakulásához az 1980-as
évek végén végzett kísérletsorozat vezetett el. Zewail eljárásával "pillanatfelvételek"
készíthetők az átmeneti állapotba került molekulákról. A "fényképezőgép"
az új lézertechnológián, a néhány tíz femtoszekundumos fényvillanásokon
alapszik. A molekulákat alkotó atomok egyetlen rezgése 10100 fs-ig tart.
A
femtoszekundumos spektroszkópia alkalmazásával megérthető és megjósolható,
hogy mi történik valójában a kémiai reakciók során.
Egyre rövidebb időtartamok felé
Fénnyel már korábban is követtek kémiai folyamatokat: egy spektrofotméterrel
és egy órával mérhető a színes anyagok átalakulási sebessége. Két angol
vegyész, Hartridge és Roughton,
1923-ban két különálló csőben beérkező oldatot egyesített, és a keveréket
egy üvegcsövön vezette el. A keverési ponttól mért különböző távolságokban
figyelték a csövet, és így a reakciót ezred másodperces részletekig követhették
nyomon.
Két 1967. évi Nobel-díjas, Ronald Norrish és George Porter, a villanófény-fotolízissel már milliszekundumosmikroszekundumos élettartamú molekulákat is tanulmányozott. A Nobel-díjat egy német tudóssal, Manfred Eigennel osztották meg, aki hasonló időfelbontást ért el úgy, hogy az oldatot nyomás-, áram- vagy hőimpulzusnak tette ki. Ismét néhány milliószoros javulást értek el a felbontásban, amikor molekulák vákuumban zajló ütközéseit vizsgálták. Ezért a munkáért Dudley Herschbach, Yuan Lee és John Polanyi kapott Nobel-díjat 1986-ban.
Mit láttak a vegyészek az időfelbontás növekedése nyomán?
Az első siker az intermedierek, az anyagok átalakulása során kialakuló
"közbülső" termékek felfedezése volt. Eleinte csak viszonylag stabil
intermediereket észleltek, de ahogy javult az időfelbontás, egyre újabb
szemeket ismertek fel a reakcióláncban: egyre rövidebb élettartamú intermediereket
is kimutattak, s egyre jobban látták a reakció lefolyását, mechanizmusát.
A femtoszekundumos spektroszkópiával már "lassított felvételen"
követhetik nyomon az átameneti állapotot.
A femtokémia a gyakorlatban
A "molekulamozihoz" Zewail vákuumkamrában keveri össze a molekulasugár
formájában beérkező reaktánsokat. Ezután egy ultragyors lézerrel, amely
néhány tíz femtoszekudumos impulzusokat bocsát ki, két impulzust ad a molekulákra.
Az első, nagy energiájú impulzus a molekulákat nagyobb energiájú állapotba
gerjeszti, és elindítja a reakciót. A második impulzus gyengébb; hullámhosszát
úgy választják ki, hogy az eredeti molekulát vagy az átalakult változatot
érzékelhessék. Ez az impulzus megadott intervallumokban érkezik a reakció
elindulása után így térképezhető fel, hogy a különböző részecskék mennyi
idő alatt jelennek meg vagy tűnnek el. A molekulákat, a kialakuló képződményeket
az ujjlenyomatként szolgáló spektrumok alapján azonosítják. Az impulzusok
közötti időtartamot a második impulzus késleltetésével változtatják: tükrökkel
kerülőútra kényszerítik. A kerülő azonban rövid, hiszen a fény 100 fs alatt
0,03 mm-t tesz meg. A folyamatok jobb megismerése érdekében az ujjlenyomatokat
és az időbeli változást kvantumkémiai számításokon alapuló szimulációkkal
vetik össze.
Az első, 1987-es kísérletsorozatban Zewail a jód-cianid bomlási reakcióját (ICN > I + CN) tanulmányozta. Munkatársaival együtt sikerült megfigyelnie az IC kötés 200 fs alatti bomlását.
Egy másik fontos kísérletben a nátrium-jodid bomlását (NaI >Na++
I) követték nyomon. A gerjesztő lézerimpulzus a Na+I
ionpárt,
amelyben az atommagok közötti egyensúlyi távolság 2,8 Ĺ (1. ábra), a gerjesztett
[Na-I]* állapotba viszi. A molekula e mellett a rövid kötéstávolság mellett
kovalens jelleget ölt. Tulajdonságai azonban megváltoznak rezgés közben:
amikor a Na és a I atomok a "külső" fordulóponton vannak, egymástól
1015 Ĺ-re, az elektronszerkezet ionons [Na+...I]*.
A rezgés kritikus ponthoz érkezik, amikor a távolság 6,9 Ĺ, mert
ekkor a gerjesztett állapot (1. ábra, fölső görbe) és az alapállapot (alsó
görbe) nagyon közel van egymáshoz: a gerjesztett [Na-I]* molekula visszaeshet
az alapállapotba, de nátrium- és jódatomokra is elbomolhat.
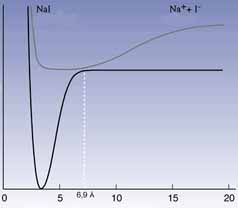
1. ábra. A NaI potenciális energia görbéi az atommagok közötti távolság
függvényében alap- és gerjesztett állapotban (alsó, illetve fölső
görbe)
Zewail és munkatársai azt tapasztalták, hogy az aktivált komplex ide-oda billegett a kovalens és az ionos szerkezet között, és ezeknek az oszcillációknak az ütemében szabad "nátriumatom-csomagok" keletkeztek. Ennek az a magyarázata, hogy a gerjesztő impulzus számos olyan gerjesztett molekulát keltett, amely 2,8 Ĺ-nél kezdte és ezután egymással szinkronban folytatta a rezgést. Ezért mindegyik ugyanakkor haladt át a bűvös 6,9 Ĺ-ön, tehát a bomlások szinte egyszerre következtek be.
Ez Zewail femtokémiájának a lényege: a femtoszekundumos impulzussal képletesen szólva Zewail megfújja a sípot és a molekulákat egyszerre indítja el a rezgési ciklusnak ugyanarról a pontjáról. A molekulák szinkronizálásának ("a koherens preparátumnak") az az egyik következménye, hogy bár a későbbi impulzussal sok milliónyi molekulát mérnek, a mozgás nem "mosódik el", hanem a koherencia miatt a molekulák úgy viselkednek, mint egy klasszikus rezgő test, például egy rugó. A mérés során az atommagok rezgés közbeni mozgása is megfigyelhető, s az átmeneti állapot nagy térbeli felbontással követhető (a NaI esetében kb. 0,1 Ĺ-mel).
Sok vegyészt foglalkoztat az a kérdés, hogy egyes kémiai kötések miért reaktívabbak a többinél, és az egyenrangú kémiai kötések egyszerre bomlanak-e fel. Zewail és munkatársai a tetrafluor-dijód-etán (F2ICCIF2 >F2C=CF2+ I2)bomlását tanulmányozva arra az érdekes eredményre jutottak, hogy a két azonos CI kötés egymás után hasad fel, az első 200 fs, a második 100-szor ennyi idő alatt.
Ugyancsak meglepő eredményt hozott a benzol (C6H6) és a jód (I2) reakciójának tanulmányozása. A két molekula, egymással ütközve, komplexet képez. A lézerimpulzus hatására a benzolról elektron ugrik át a jódra: a benzol pozitív, a jódmolekula negatív töltésű lesz. A két jódatom közötti kötés megnyúlik, mivel a benzolhoz közelebbi jódatomot a benzol magához vonzza. A kötés végül elszakad, és a másik jódatom lerepül. Mindez 750 fs alatt játszódik le. Zewail kimutatta azonban, hogy nemcsak így képződnek jódatomok. Néha egy elektron "visszahullik" a benzolra. A jódnak azonban már késő: a molekula szétszakad, mint a túlfeszített gumiszalag, és mindkét jódatom lerepül. A kísérletek azt illusztrálják, hogy a korábban feltételezettnél bonyolultabb reakciómechanizmusokkal kell számolnunk.
Gyakran tanulmányozott modellreakció a ciklobután gyűrűnyitási reakciója, amelynek során etilén keletkezik. A reakció lejátszódhat egyetlen átmeneti állapot kialakulásával, de két lépcsőben is úgy, hogy intermedierként tetrametilén képződik, s csak egy újabb gát átlépése után keletkezik a végtermék. Zewail és csoportja kimutatta, hogy valóban létrejön az intermedier, és élettartama 700 fs.
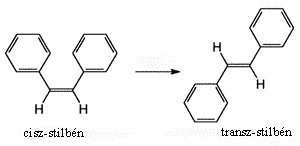
Ugyancsak femtoszekundumos spektroszkópiával tanulmányozták a stilbénmolekula fotoizomerizációját: a cisz-forma átalakulását transz-változattá. A lézerimpulzus hatására a cisz-izomer kettős kötése meggyengült, ezért mindkét benzolgyűrű egyszerre elfordulhatott 90 fokkal, és így mintegy 300 fs alatt megcsavarodott intermedier keletkezett, majd végül kialakult a transz-változat. Hasonló, fotogerjesztéssel kiváltott, koherens csavarodást figyeltek meg más kutatók a retinál molekulán, amely a szem pálcikáiban levő rodopszin színes anyaga. Amikor fényt érzékelünk, a legfontsabb fotokémia lépés a retinál kettős kötésének cisz-transz átalakulása. A folyamat időtartama 200 fs. A reakció sebessége arra utal, hogy az elnyelt foton energiája nem oszlik el, hanem a kettős kötésen lokalizálódik. Ez magyarázatot adhat arra, hogy a szem miért lát jól éjszaka is.
A femtoszekundumos spektroszkópiával ma már felületeken, oldatokban, polimerekben, biológiai rendszerekben is végeznek vizsgálatokat. A kémiai reakciók mechanizmusának ismerete nemcsak elméleti okokból, hanem a reakciók szabályozásának szempontjából is fontos.
A femtokémia alapvetően megváltoztatta a kémiai reakciókról alkotott képünket. Az "aktiválás", "átmeneti állapot" kifejezések mögött ma már az egyes atomok mozgását is láthatjuk. Zewail kutatásai robbanásszerű fejlődést indítottak el a kémiában.
Az oldal forrása: http://www.kfki.hu/~cheminfo/hun/olvaso/nobel99/femto.html
Az Eötvös Loránd Tudományegyetem Kémiai Tanszékcsoportjának Fizikai-Kémiai Tanszékvezetője által írt és a Természet Világában megjelent cikke olvasható a következő Internet címen:
http://www.kfki.hu/chemonet/TermVil/tv2000/tv0001/femto.html
Az oldal forrása: http://www.sulinet.hu/cgi-bin/db2www/lm/frame/cikk?id=1000&kat=bnb